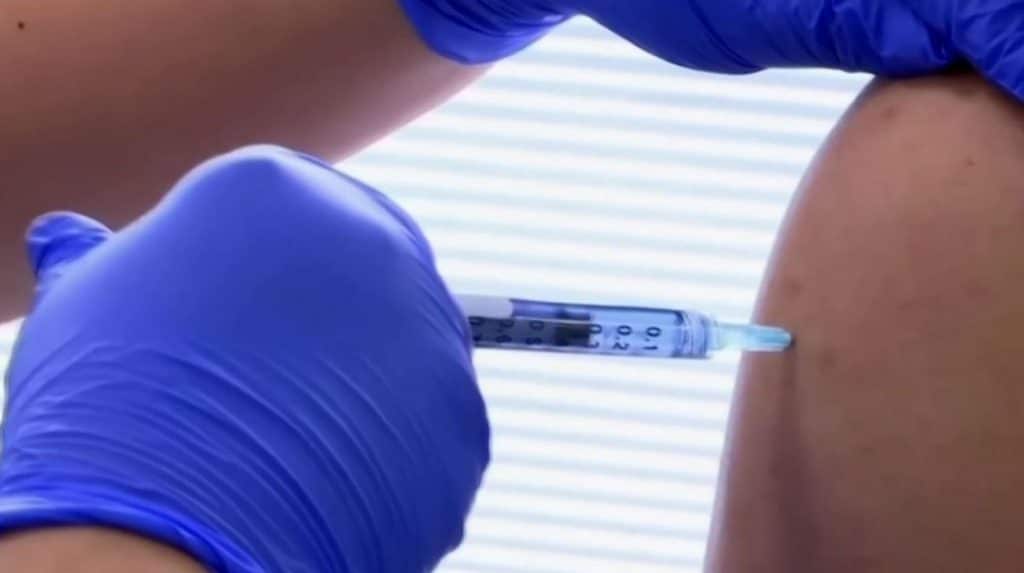
A Agência Nacional de Vigilância Sanitária (Anvisa) suspendeu as pesquisas com vacina CoronaVac, desenvolvida farmacêutica Sinovac e em testes clínicos em parceria com o Instituto Butantan, após o falecimento de um voluntário. A decisão foi anunciada na segunda-feira (09), causou estranheza e entrou para o epicentro de uma disputa que tem tudo com política e nada com ciência – muito menos saúde pública.
Órgão técnico da Anvisa, a Gerência Geral de Medicamentos (GGMED) mandou parar os trabalhos a partir de dados insuficientes e sem consultar o colegiado de diretores da agência. A falta de sintonia é tamanha, que a Comissão Nacional de Ética em Pesquisa (Conep) recomenda a continuidade dos testes. Para que um medicamento seja testado e autorizado no Brasil, é preciso aval tanta da Anvisa quanto da Conep, ligada ao Conselho Nacional de Saúde (CNS), do Ministério da Saúde.
Interrupções e reavaliações são comuns em pesquisas que envolvam voluntários. O que piorou o quadro foi a declaração do presidente Jair Bolsonaro contra o governador João Doria (PSDB). “Morte, invalidez, anomalia. Esta é a vacina que o Doria queria obrigar a todos os paulistanos tomá-la”, escreveu Bolsonaro, desmerecendo abertamente e sem provas o imunizante de origem chinesa.
O presidente, todavia, omitiu que a vacina de Oxford, desenvolvida pela anglo-sueca AstraZeneca e também em testes no Brasil com recursos federais e parceria com Fundação Oswaldo Cruz (Fiocruz), também apresentou episódios suspeitos depois descartados. Uma das supostas vítimas fatais era um médico brasileiro que recebeu placebo. Bolsonaro tem aberta predileção por uma solução americana ou europeia para a pandemia, deixando de lado que a CoronaVac é a mais adiantada nos testes. Além dela e da alternativa da AstraZeneca, pelo menos outras duas vacinas estão em estudos no país por meio de parcerias com laboratórios internacionais.
O caso ganhou contornos mais constrangedores após a divulgação, no início desta terça-feira (10), que o “evento adverso grave” relatado não teria relação com a vacina. O voluntário, um homem de 33 anos, teria cometido suicídio em 28 ou 29 de outubro, acredita a Polícia Civil, que encontrou o corpo em uma residência. O Boletim de Ocorrência, emitido na tarde de 29 de outubro, antes da discussão surgir, já indicava “suicídio consumado”. Representantes do governo de São Paulo demonstraram indignação com a medida e defenderam que a morte não teve relação alguma com o imunizante.

A expectativa do diretor do Instituto Butantan, Dimas Covas, é que após os esclarecimentos, a Anvisa autorize a retomada dos estudos ainda nesta semana. Ele também lembrou que as autoridades federais foram comunicadas sobre o episódio na sexta-feira (6). Porém, como ainda não foi concluído o laudo da necropsia determinando a causa da morte do voluntário, no final desta tarde a Anvisa anunciou que a paralisação estava mantida. “Quando temos eventos adversos não esperados, aqueles que no primeiro momento não conseguimos estabelecer uma correlação, a sequência de eventos é uma só: a interrupção do estudo”, afirmou o presidente da agência, Antonio Barra Torres.
O vice-presidente, Hamilton Mourão (PRTB), afirmou que “todo e qualquer processo de vacina sofre avanços e recuos”. Mourão se esquivou de comentar o teor das declarações de Jair Bolsonaro.